今年7月27日,SIM0278临床试验获国家药监局批准,适应症为中重度特应性皮炎(Atopic dermatitis, AD)。先声药业积极筹备临床研究,一个月内即快速达成首例受试者用药的里程碑新进展,入组速度行业领先。若得到临床验证,SIM0278或可有效弥补目前已获批特应性皮炎治疗手段的不足,满足患者连续长期用药的临床需求。
特应性皮炎是一种慢性、复发性、炎症性皮肤病,常见临床特征包括皮肤干燥、红斑、水肿、糜烂、表皮剥脱、苔藓样变等[1]。根据弗若斯特沙利文数据统计,2019年全球AD患者量已达6.49亿人,2030年则预期增至7.55亿人。目前虽已有多种治疗方式用于缓解或消除AD临床症状、减少和预防复发,但外用药物疗效有限,免疫抑制剂、生物制剂等则存在多种不良反应或风险 [2-5],临床仍需要更安全有效的治疗药物以满足患者控制疾病和长期治疗的需求。
研究显示,调节性T细胞(Treg)参与AD的发病机制。Treg在免疫耐受和免疫调节中发挥重要作用,已被证明是皮肤过敏反应中炎症下调和外周维持免疫耐受的关键。白介素-2(IL-2)参与Treg的分化、扩增和存活 [6]。
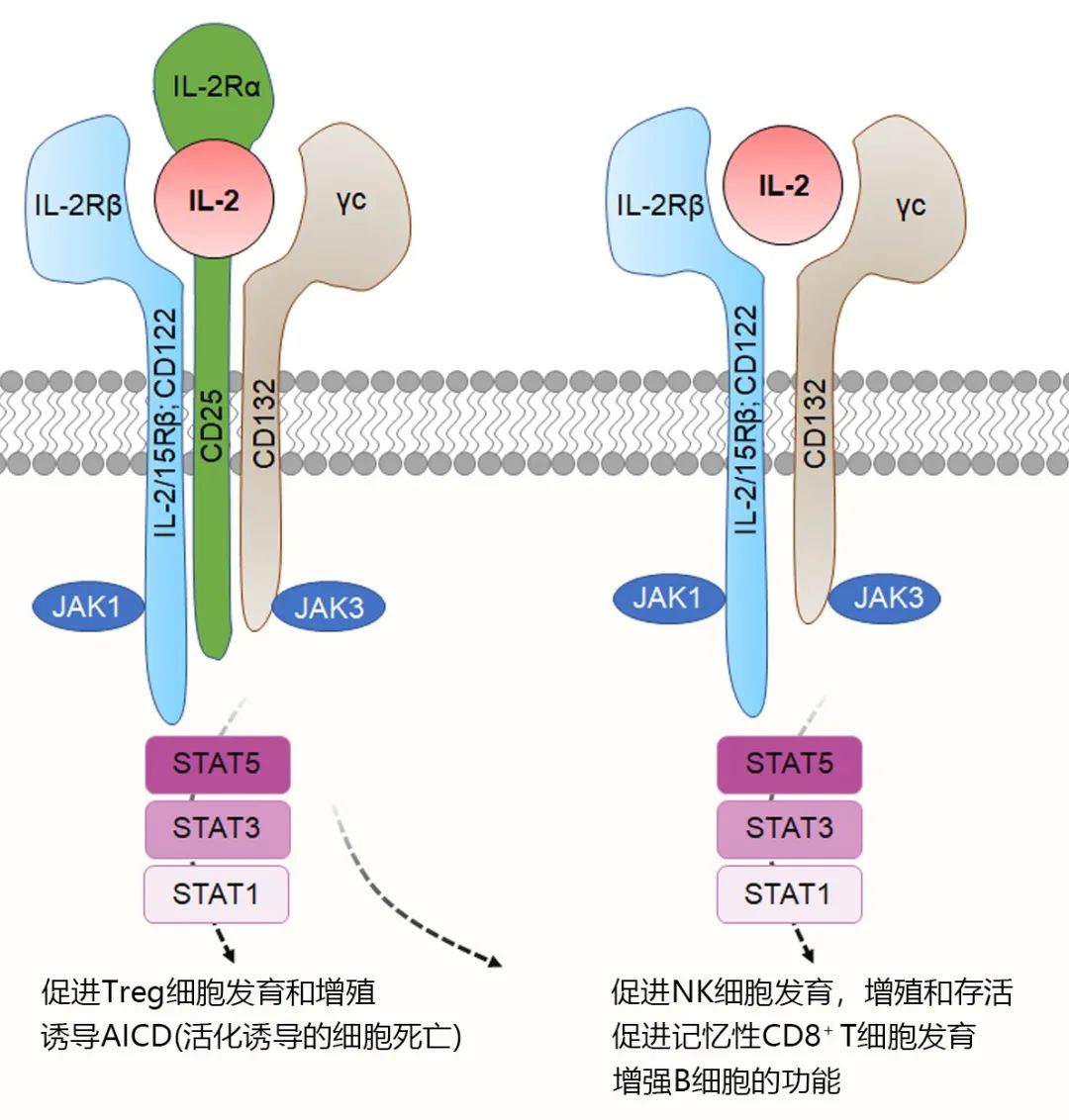
IL-2 的信号通路 (制图:先声药业 体外药理部 付勇)
先声自有蛋白质工程平台开发的SIM0278是一种Treg偏好型IL-2突变的Fc融合蛋白,通过引入相应突变,降低了SIM0278与效应T细胞的亲和力,但保留了与Treg细胞的高亲和力,进而提高了对Treg细胞的选择性。
临床前研究显示,SIM0278在体外可选择性地激活Treg细胞,对效应T细胞和自然杀伤细胞无影响,从而达到恢复机体免疫平衡的作用。
除了已经获批的AD适应症,SIM0278还拥有多种自免疾病的潜力,国内潜在可开发适应症患者逾千万。同时SIM0278临床前试验显示,其拥有疗效更强、更持久且药物使用更安全的潜力。
2022年9月,先声药业以4.92亿美金总里程碑付款,将SIM0278海外开发及商业化权益独家授权给Almirall公司。目前SIM0278海外适应症探索也在同步布局,合作伙伴正积极筹备美国临床研究。
本次SIM0278的全球首次人体用药,是该项目奔赴帮助全球患者目标历程中迈出的重要里程碑。先声将继续与合作伙伴携手全力推动SIM0278在全球的临床验证,期待早日为全球自身免疫疾病患者,带来治疗新选择。