2020年11月18日,中国国家药监局药品审评中心(CDE)最新公示,先声药业(2096.HK)创新药SIM1909-13片获得临床试验默示许可。
痛风是一种常见的代谢性疾病,是单钠尿酸盐(MSU)沉积所致的晶体相关性关节病,与嘌呤代谢紊乱和 (或)尿酸排泄减少所致的高尿酸血症直接相关。痛风可并发肾脏病变,严重者可出现关节破坏、肾功能损害,常伴发高血脂症、高血压病、糖尿病、动脉硬化及冠心病。目前国内高尿酸血症患者的发病率为10%,约有1.3亿的潜在人群。痛风患病率也呈现上升趋势,患者约在3200万人,已成为中国第二大代谢类疾病。
URAT1抑制剂是一种新的痛风治疗在研药物,其通过选择性地抑制URAT1对尿酸的再吸收及增加尿酸的排泄,有效控制血液尿酸水平,目前中国尚无获批销售的URAT1选择性抑制剂。
据文献报导,SIM1909-13片是对URAT1的高选择抑制剂,排除了对OAT1/3的选择抑制作用可能有助于提高其安全性,临床前数据显示其相比苯溴马隆降尿酸疗效更显著且肝肾副作用可能更低。
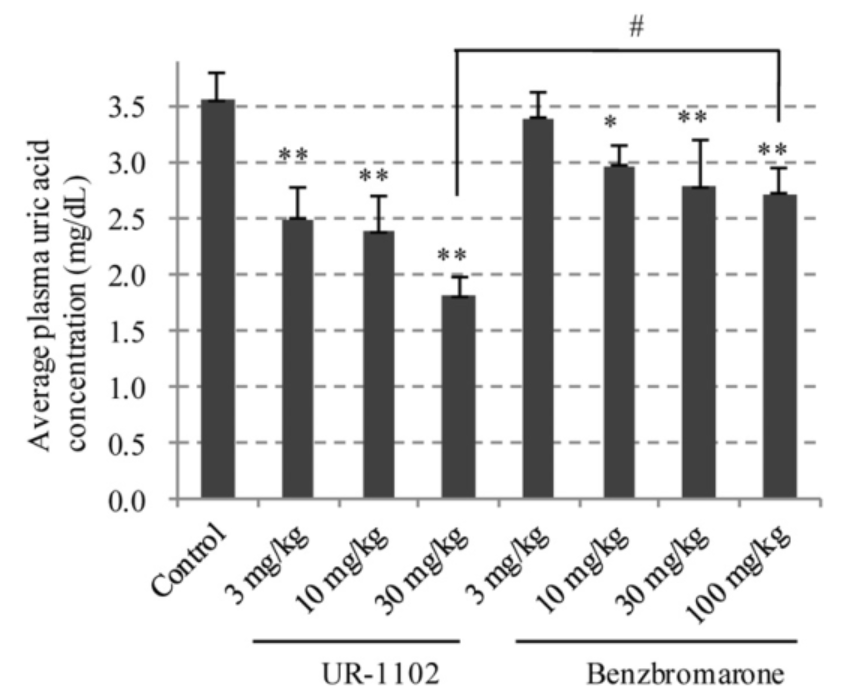
UR-1102(URC102)临床前数据,来源:J Pharmacol Exp Ther 357:157–166, April 2016
此外,一项随机、双盲、安慰剂对照的I期研究,以评估其安全性和耐受性的临床试验中入组了31名韩国人和23名白种人,结果显示SIM1909-13片在3-10mg剂量范围内具有显著降低血尿酸水平的疗效且具有良好安全性,并具有剂量依赖性特征。
目前主要的降尿酸药物包括别嘌醇、非布司他和苯溴马隆,2019年中国市场规模超20亿元,近几年保持高速增长。
前瞻性陈述
本新闻稿中提供的信息包含前瞻性陈述,其中涉及许多已知和未知的风险、不确定性和假设。此处包含的前瞻性陈述反映了先声药业截至本新闻稿发布之日的判断和观点。此类前瞻性陈述既不是承诺也不是保证,而是受到各种风险和不确定性的影响,其中许多风险和不确定性超出了我们的控制范围,或可能无法实现,并且可能导致实际结果与这些前瞻性陈述中的预期结果存在重大差异。我们明确表示不承担任何义务或承诺公开发布任何此类声明的任何更新或修订,无论是由于新信息、未来事件或其他原因,以反映我们预期的任何变化或任何此类声明所依据的事件、条件或情况的任何变化。